研究内容
私たちの細胞内では、役目を終えて不要になったり、異常なタンパク質は選択的に分解されています。ユビキチン・プロテアソーム系は細胞内で不要になったタンパク質や異常タンパク質を分解するシステムです。ユビキチン・プロテアソーム系の破綻はがんや炎症疾患、神経変性疾患、老化など、様々な病態につながることが知られています。私たちは、特定のタンパク質が特定のタイミングで分解される原理=「タンパク質分解コード」の解明により、疾患の発症機構の正確な理解と治療への貢献を目指します。
さらに近年、「標的タンパク質分解」が次世代の創薬コンセプトとして脚光を浴びています。標的タンパク質分解はユビキチン・プロテアソーム系を利用して、がんなどの疾患原因タンパク質を分解により細胞内から除去する新技術です。現在、がんの治療薬として臨床試験が行われれるなど、国際的に開発が進んでいます。しかしこの技術を確立するためには作用メカニズムの解明が不可欠です。私たちは「タンパク質分解コード」に立脚して、薬剤の標的タンパク質がいかにして効率良く分解されるのかを解明し、創薬応用につなげる研究=「分解創薬学」に取り組んでいます(一部は特許出願済み)。
学生の方・一般の方へ
1. タンパク質分解コードの解明
細胞内で不要になったタンパク質は分解され、新しく合成されたタンパク質に置き換わっています。このようなタンパク質の分解は、細胞内シグナル伝達や、遺伝子発現、エピゲノム制御、炎症応答、DNA修復など、細胞が正常に機能する上で不可欠です。
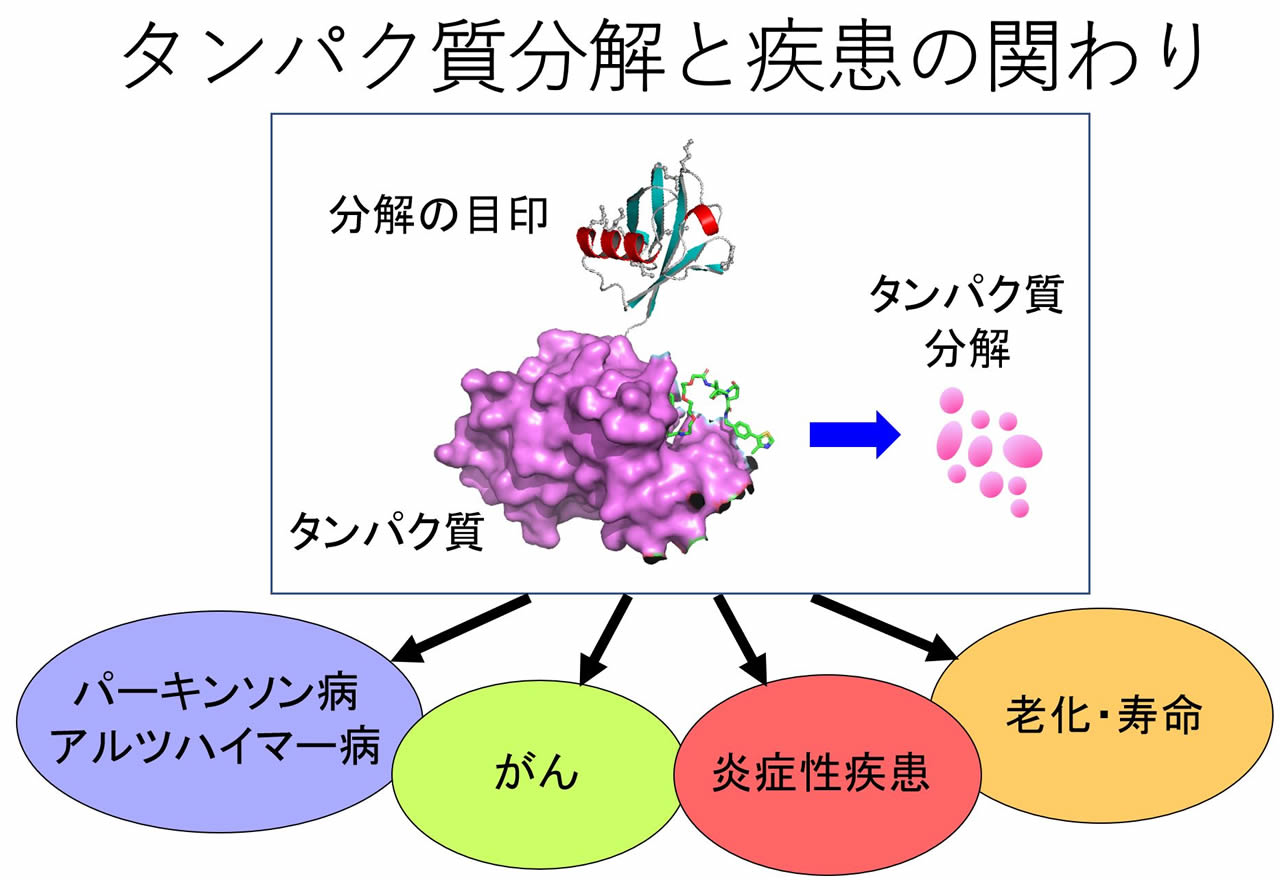
分解されるべきタンパク質を選別するための目印(タグ)の役割を果たすのが「ユビキチン」です。不要になったタンパク質は、ユビキチン付加酵素によって、ユビキチンを付加されます(ユビキチン化と呼ばれる)。ユビキチンを付加されたタンパク質は、タンパク質分解酵素である「プロテアソーム」へと運ばれて、分解されます。この経路は「ユビキチン・プロテアソーム系」と呼ばれています。ユビキチン・プロテアソーム系は細胞内で不要になったタンパク質や異常タンパク質を分解するシステムです。ユビキチン・プロテアソーム系の破綻はがんや炎症疾患、神経変性疾患、老化など、様々な病態につながることが知られています。
では、特定のタンパク質が特定のタイミングで分解されるメカニズムはどうなっているのでしょうか?私たちは、タンパク質には自身の寿命や、どのようなタイミングで分解されるか、という情報が「分解コード」として刻まれていると考えています。この「分解コード」の成り立ちを解明し、その異常がどのようにしてがんや神経変性疾患などの疾患につながっていくのかを明らかにしたいと考えています。
2. タンパク質分解創薬への応用
私たちの細胞内には、がん細胞の生存や増殖にとって有利に働くタンパク質が存在します。このようなタンパク質はがんの治療標的であり、薬剤によって阻害できればがん細胞の細胞死を引きおこすことができます。
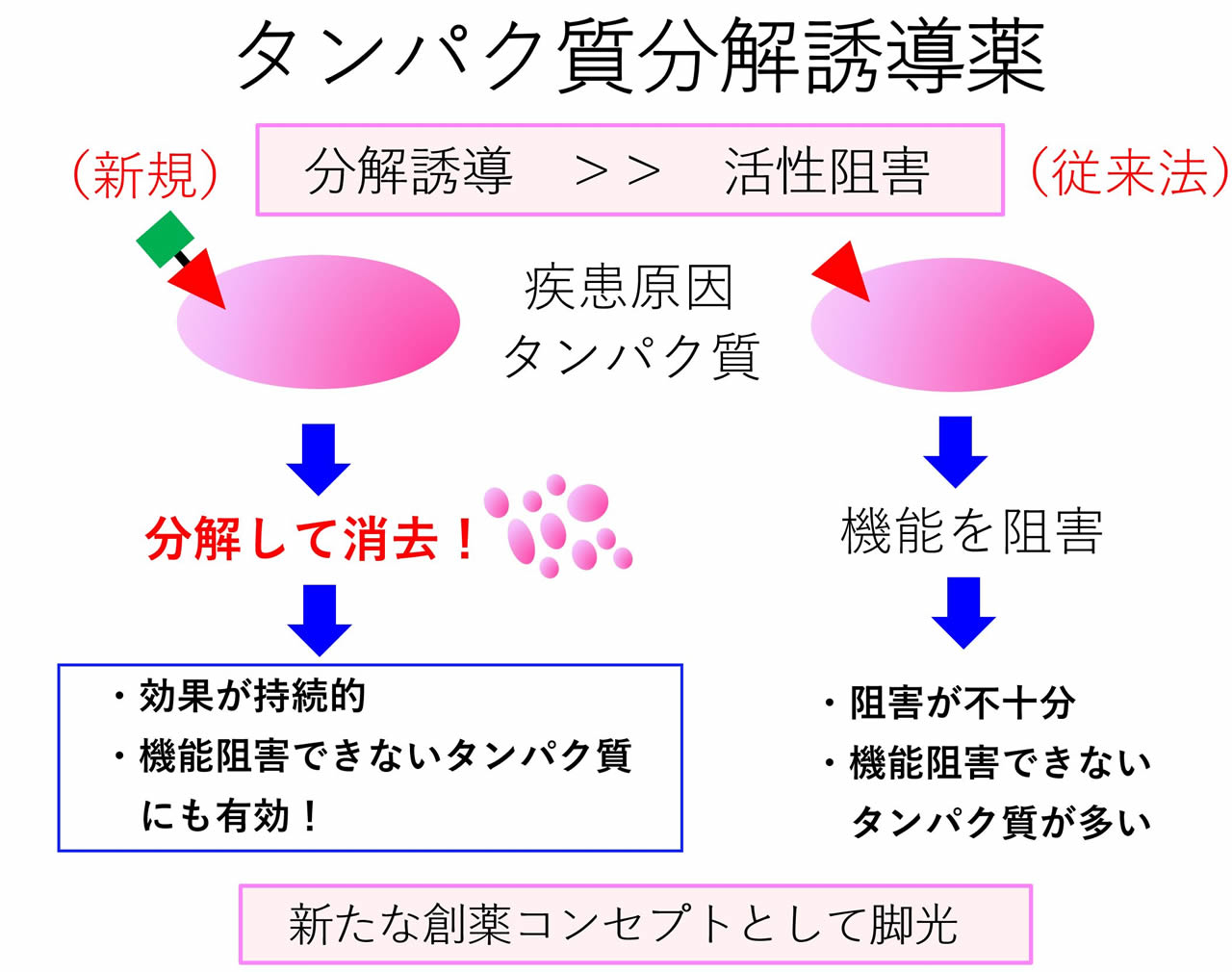
このような治療標的タンパク質が数多く存在しますが、いわゆる阻害薬など既存の薬剤の標的となっているタンパク質は一部であり、それ以外の多くのタンパク質は薬剤によって阻害できませんでした。これに対して、標的タンパク質を細胞内で分解して除去する「標的タンパク質分解創薬」が、創薬ターゲットの範囲を大幅に広げる革新的な創薬コンセプトとして脚光を浴びています。
標的タンパク質分解の原理は、細胞内にもともと備わっているユビキチン・プロテアソーム系を利用するものです。特殊な薬剤(分解薬)によって標的タンパク質のユビキチン化を誘導すれば、細胞内で狙ったタンパク質を分解することが可能になります。代表的な薬剤として、多発性骨髄腫の治療に使われているレナリドミドなどがあります。また、乳がん、前立腺がんに対する分解誘導薬が臨床試験に入っています。
私たちは、標的タンパク質分解のメカニズムを明らかにしたいと考えています。標的タンパク質分解の作用メカニズムには不明な点が多く残っています。分解に関わる制御因子を明らかにすることができれば、薬剤の効き目をがんの種類や患者ごとに事前に予測するオーダーメイド医療につながっていく可能性が考えられます。また、将来的に特定の制御因子の存在量を増やしたり活性を増加させる方法が見つかれば、がんに対するより高効率な治療薬につながると考えられます。実際に私たちは分解創薬の効果を促進する化合物を複数見出すことに成功し、作用メカニズムの解明を進めています(特許出願済み)。
3. 学生のみなさんへ
私たちの研究室では、学生のみなさんには最先端の研究テーマに取り組み、新たな現象の第一発見者になってほしいと思っています。また4年生で学会発表すること、卒論の内容を学術論文として発表することを目指し、研究を発信する・議論する力も身につけていけるよう指導しています。
研究者・専門家の方へ
1. ユビキチン・プロテアソーム系によるタンパク質分解機構の解明
ユビキチン修飾は生体に必須の翻訳後修飾であり、極めて広範な細胞内機能を司っています。ユビキチン自身が連結したポリユビキチン鎖は連結様式の違い (K6, K11,K27, K29, K33, K48, K63, M1を介して連結) により、異なる解読分子(デコーダー)によって認識され、K48鎖によるプロテアソーム依存性タンパク質分解の制御、K63鎖による免疫応答シグナル伝達やDNA修復の制御など、多彩な経路を制御します。こうした機能的多様性は「ユビキチンコード」と称されています。
従来、単一の連結タイプからなるユビキチン鎖(例えばK48鎖やK63鎖)はそれぞれ別個に機能すると考えられてきました。しかし、異なるユビキチン鎖の発するシグナルがどのように相互連関して複雑な細胞応答をもたらすのかはよくわかっていませんでした。
私たちは、一つのユビキチン分子内の2か所のリジンが連結に使われることで「枝分かれ」した鎖(分岐鎖)が細胞内に豊富に存在すること、細胞内シグナル伝達に関与することを見出してきました (Ohtake et al., Molecular Cell 2016; Ohtake et al., PNAS 2018; Ohtake et al., Methods Enzymol 2019; Ohtake et al., TIBS 2020)。その後の私たちを含む国内外の研究により分岐鎖の様々な機能が報告され、分岐鎖はユビキチンコードの概念を拡大する新たなコンセプトとして認知されつつあります。しかし、ユビキチン鎖を枝分かれさせる分岐鎖形成酵素や、分岐を認識するデコーダー分子については大部分が未知であり、そのため、分岐鎖が単なるシグナルの足し算ではなくそれ自身が固有の機能を有するのか、いまだ十分に解明されていません。
そこで私たちは、分岐鎖の形成に関わる新たな酵素の発見 (Soma-Kaiho et al., Molecular Cell 2021)、複雑な構造の分岐鎖の発見 (Akizuki et al., Nature Chem Biol, 2023) など、分岐鎖が担う細胞内機能の解明に取り組んでいます。

2. 化合物による標的タンパク質分解のメカニズムの解明
化合物によって誘導される標的タンパク質分解は、次世代の創薬コンセプトとして注目されています。2019年より、ホルモン受容体の分解誘導薬が前立腺がん、乳がんに対する治療薬として臨床試験に入るなど、国際的な開発競争が激化しています。標的タンパク質分解の原理は、標的タンパク質に対するリガンドとユビキチンリガーゼ(VHLなど)に対するリガンドとをリンカーでつないだ化合物(分解誘導剤、PROTAC)あるいは標的タンパク質とユビキチンリガーゼ(CRBNなど)の相互作用を誘導する化合物(分子糊、Molecular Glue)によって両者を近接させ、標的タンパク質を強制的にユビキチン化することで分解を誘導するというものです。すなわち、細胞が本来有しているユビキチン化機構を「ハイジャック」すると一般には考えられています。
しかし、標的タンパク質分解の詳細なメカニズムは十分にはわかっていません。ユビキチン依存的なタンパク質分解は基質とリガーゼの複合体形成だけでなく、多様な高次構造のポリユビキチン鎖(ユビキチンコード)の形成、特定のポリユビキチン鎖を認識するデコーダータンパク質によるプロテアソームへの基質運搬など多段階で調節されていると考えられます。そこで私たちはユビキチンコードの観点から標的タンパク質分解のメカニズム解明を試みています。メカニズムが明らかになれば、より高効率、高精度な分解誘導技術の開発につながると考えられます。
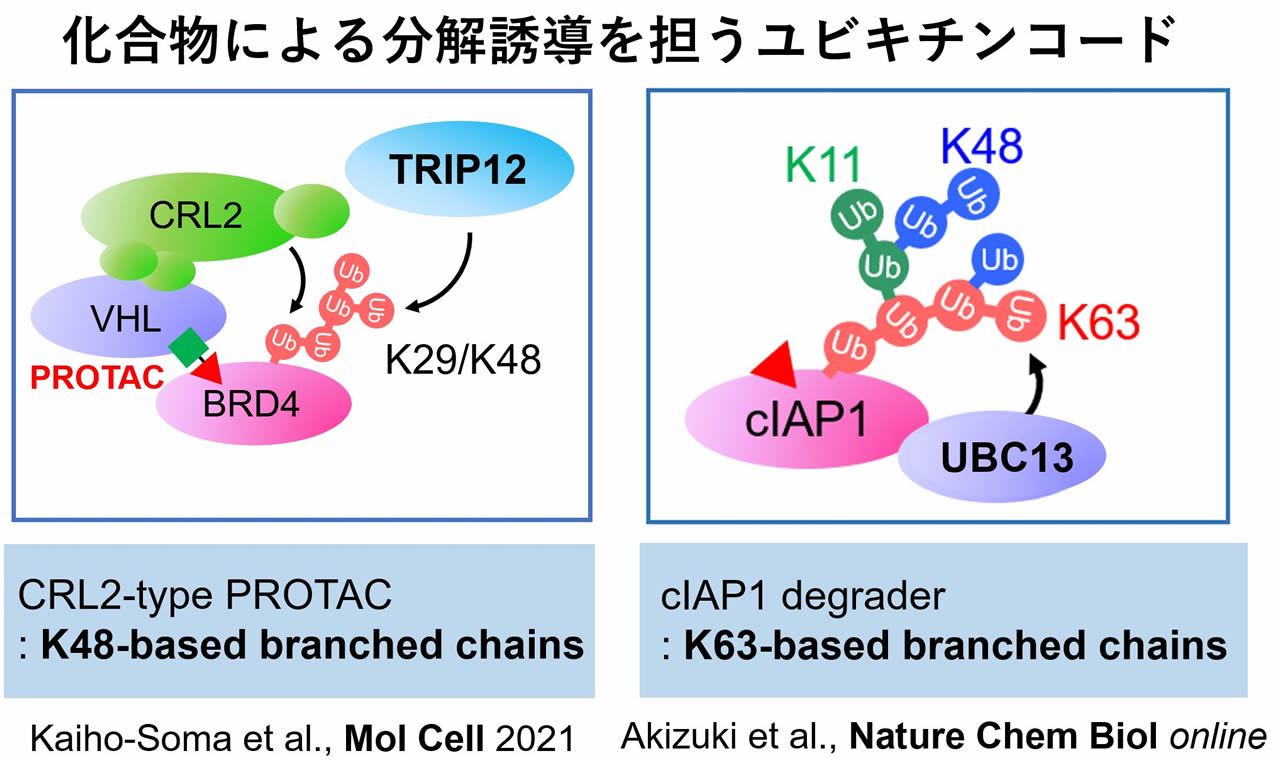
私たちは最近、標的タンパク質分解を促進するユビキチンリガーゼとしてTRIP12を見出しました。TRIP12はK29連結型ユビキチン鎖(K29鎖)を特異的に伸長する酵素活性を有することが判明しました。詳細な解析の結果、TRIP12はPROTAC依存的にBRD4およびCRL2VHL複合体にリクルートされ、K29鎖を特異的に付加することで、CRL2VHL複合体と協調的にK29/K48分岐鎖を形成し、BRD4の分解を促進することが明らかとなりました。
私たちの研究で、標的タンパク質分解誘導において形成されるユビキチンコードの一端が初めて明らかとなりました。分岐鎖はプロテアソーム依存性分解を促進すると考えられているため、PROTACによる分岐鎖形成は、本来分解されにくいタイプの標的基質の分解に適していると考えられます。PROTACの作用に関与する共役因子やユビキチンコードの解明は、将来的により高活性な薬剤の開発に貢献することが期待されます。さらに私たちはPROTACの効果を促進する化合物を発見し、作用メカニズム解明を進めています(特許出願済み)。
秋月 慶乃さん
- Comment -
学生のうちに研究の成果を発表する機会をえて、研究のモチベーションが高まりました。
時間がかかる実験や、工程が多い実験が成功したときは、特にその喜びが大きいです。
予想外の結果が出たときでも、どうしてその結果が出たのかを考えるのも研究の面白さだと思います。
森 友紀さん
- Comment -
研究の楽しさだけでなく、遊ぶことの大切さも実感しました。研究発表が終わった後などは思う存分遊んでリフレッシュしています。そのメリハリを常に心がけ、遊んだ3倍は実験することをモットーに研究生活を送っています。
(コンサル会社内定)
千葉 崚太郎さん
- Comment -
在学時は、分岐型ユビキチン鎖の基礎研究を行っていました。自分で手を動かして仮説を検証し、良い結果が出た時の達成感は何事にも変え難く、研究の醍醐味の1つです。
卒業後は研究活動で培った経験を活かして、これらの研究が、製薬業界と患者をつなぐ架け橋になるような仕事に取り組みます。
齋藤 惠利沙さん
- Comment -
実験が思うように進まないことも多いですが、少しずつデータがそろっていく過程にやりがいを感じています。 薬学科では国家試験に向けた勉強との両立が欠かせません。計画的に取り組むことで、短い時間で集中して研究活動を行っています。