研究紹介
生命を理解しようとする試みとして始まった有機化学は、生物と物質を繋ぐサイエンスとしての重要性を保ち続けています。生物を構成する主な物質は、有機化合物であり、それらが生体内でどのように働くかは有機化学の観点から理解できます。一方、有機化学は、自然を理解するだけの学問ではなく、新しい分子をデザインし、つくり出すことができる点で、科学の中でも独特の位置を占めています。
2019年4月よりリニューアルした生体分子有機化学研究室では、生物活性を持つ有機分子に新しい機能を付加する試薬の開発、生物活性を持つ有機分子が生体に作用する仕組みの解明、これまでに無い新しい形を持つ有機分子の構築法の開発、新しい原理に基づく有機分子構築法の開発などを通して、生体に作用する新しい有機分子の創造を目指しています。
最近の研究
学術論文として最近発表した研究を紹介します。
標的タンパク質分解誘導薬に機能を追加する
標的タンパク質分解誘導薬とは、細胞内に備わるユビキチンープロテアソーム系(主要なタンパク質分解系の一つ)を利用して、細胞内から無くしたい標的タンパク質(疾病原因タンパク質など)を選択的に分解へと誘導する薬剤です。標的タンパク質分解誘導薬は、標的タンパク質に選択的に結合する小分子(標的タンパク質リガンド)と、E3ユビキチンリガーゼと呼ばれる酵素に選択的に結合する小分子(E3リガンド)を結合させたキメラ型構造を持っています。この薬剤を用いた標的タンパク質分解技術は、近年、疾病治療の新しい形態(モダリティ)として世界中で注目を集めています。
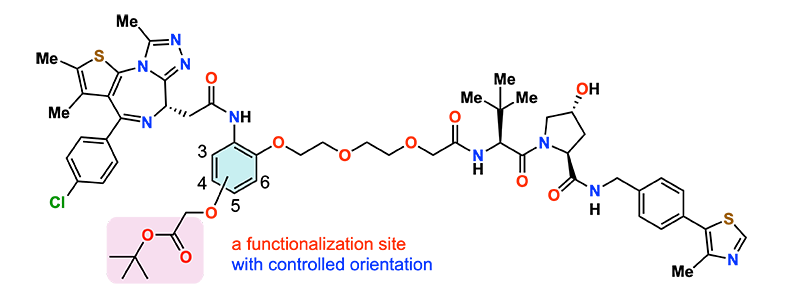
私たちは、標的タンパク質とE3ユビキチンリガーゼに結合できるという標的タンパク質分解誘導薬が持つ二つの機能に加えて、更なる機能性分子を追加できる分子を設計し、創製しました。この新しい分子には、3次元的な方向性を明確に規定しながら機能分子を追加できます。適切な機能性分子を導入すれば、標的タンパク質分解誘導薬の作用機作解析への利用や活性向上が期待できます。
脱芳香族化を伴ったジアステレオ選択的なダブルスピロ環化反応
脱芳香族化を伴った官能基化反応は、入手容易な置換ベンゼン誘導体を、複雑な骨格をもつ化合物へと短工程で導くことができる有用な反応です。最近では、複数の結合形成反応への応用例が注目を集めていますが、これまでに立体選択性に関する報告はほとんどありませんでした。このような背景から、私たちは、脱芳香族化を伴ったジアステレオ選択的なダブルスピロ環化反応を開発し、N-aryl propiolamide から一挙に trans-ジアザジスピロ環骨格(trans-diazadispirocycle)を構築することに成功しました。
二つの環が、ただ一つの原子を介して結合している場合に、その原子をスピロ中心と呼びます。今回合成した骨格は、スピロ中心と窒素原子を二つずつ持つことから、「二つ」を意味する「ジ」を付けて、ジアザジスピロ環骨格と呼んでいます。窒素原子などのヘテロ原子を含むスピロ骨格は、近年幅広い分野で注目を集めています。例えば、医薬品を設計する場合に、活性増強や物性改善、新規性付与を期待して、スピロ環骨格が用いられることがあります。
今回開発した方法を用いることで合成できる trans-diazadispirocycle は、既存法では合成困難な骨格を持つことから、次世代のスピロ環化合物として、創薬研究分野での応用が期待できます。

刺激を与えると異なる構造と生物活性を持つ分子に変化する人工多能性幹分子の創製研究
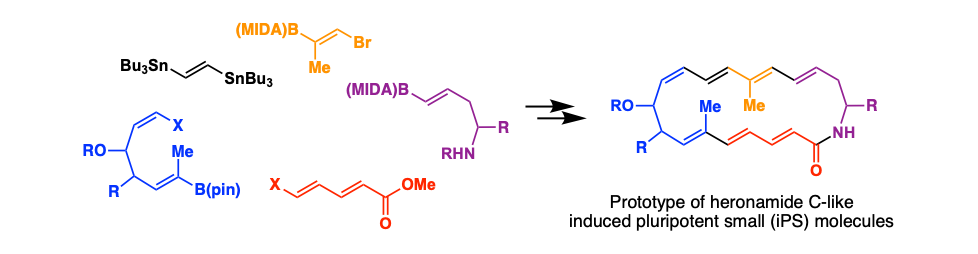
天然からは変わった構造と興味深い生物活性を有する化合物がしばしば単離されます。例えば、放線菌より単離された抗真菌性ポリエンマクロラクタム(大環状構造を持つラクタム化合物)であるheronamide Cは、酸素雰囲気下加熱すると、二重結合の酸化、ピロリジン環の環化、続く[6 + 4]付加環化反応を経てheronamide Aに変化します。一方、紫外線を照射すると[6 + 6]付加環化を経てheronamide Bに変化します。他にも、このような反応を経て、異なる生物活性を持つポリエンマクロラクタム化合物が発見されています。

我々は、これらの天然物にヒントを得て、異なる環境または刺激に晒すと、異なる構造と生物活性を持つ分子に変化するスマート分子が創製できれば、将来の医薬などへの展開が可能なのではないかと考えました。我々はこれらの合成分子を、京都大学の山中先生らにより作製された、様々な組織の細胞に分化できる人工多能性幹細胞(induced pluripotent stem cells)になぞらえて、人工多能性小分子(induced pluripotent small molecules)と捉え、その実現可能性を探索しています。
最近、heronamide C型の環構造を持つ人工マクロラクタム分子を、部分構造を連結しながら合成できるモジュラー型合成法を確立しました。この方法論を展開することで、人工多能性小分子の創製を目指しています。
生物活性分子を修飾する反応剤と反応の開発
既存の薬剤(生物活性分子)に新たな機能を付加することで、その薬剤の活性や標的選択性を改変したり、もとの薬剤の作用機作解析を容易したりすることが可能です。最近、私たちはフッ素を含んだプロパルギル基を生物活性分子に導入する反応剤と試薬を開発しました。
また、新しく見つけた試薬の反応性を利用して、自由なアイデアのもとで新規反応の開発も行っています。
最近の研究(池内)
神経毒性を持つ天然物の合成研究
自然界に存在する植物は、様々な生物活性を示す天然物を生合成しています。古代の人類はそれらを薬用植物として利用していましたが、中には神経毒性を持つ植物が存在することも学びました。日本三大有毒植物として位置付けされているドクウツギ、ドクゼリ、トリカブトがその代表例です。これらの植物および毒性本体である天然有機化合物は、現在でも研究者の注目を集めています。
私たちはこの中でドクウツギに含まれるコリアミルチン類の化学合成を目指した研究を行なっています。セスキテルペンに分類されるコリアミルチンは炭素5員環と炭素6員環がcis縮環しており、エポキシドなど複数の官能基がこの二環性骨格上に置換しています。このような高度に官能基化された天然物は化学合成が難しいですが、最近私たちは2-メチル-1,3-シクロペンタンジオンから多段階合成を経てコリアミルチンの全合成を達成しました。本合成の鍵反応に、1,3-シクロペンタンジオン構造の非対称化を伴う分子内アルドール反応を利用しています。すなわち、反応基質であるアルデヒドに存在する二つの反応点、カルボニル炭素(ピンク及び水色ハイライト)のうち、前者のみを選択的に反応させています。プロリン誘導体触媒の使用がこのような選択性をもたらしています。
現在、確立した合成経路を利用してコリアミルチンの類縁天然物、ツチン、デンドロビン、コリアンラクトンなどの合成を検討しています。

酸素置換シクロペンタジエンの特性を利用する新規反応の開発
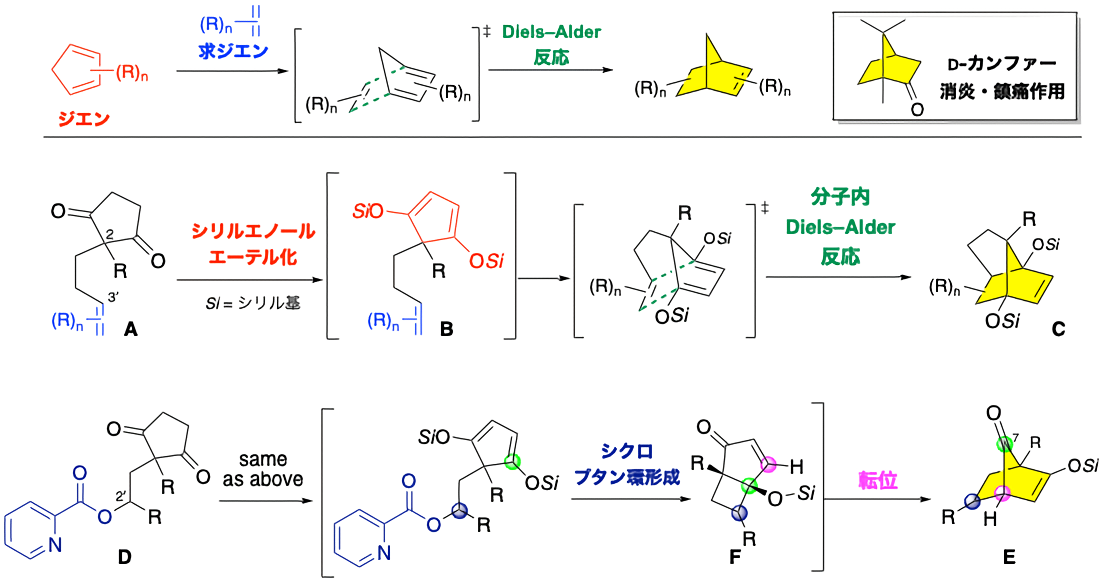
シクロペンタジエンは反応性が富んでおり、Diels–Alder反応のジエンとして汎用されています。Diels–Alder生成物はD-カンファーの母骨格であるビシクロ[2.2.1]ヘプタン(ノルボルナン)骨格を含んでいますが、本骨格は天然物にも見られます。しかし、そのほとんどがノルボルナン骨格上に多数の官能基が置換しており、別の炭素環がノルボルナン骨格上に縮環しています。そのため、複雑なノルボルナン骨格を含む複雑分子を簡便に構築する方法論の開発が現在の有機合成の重要課題となっています。
私たちは2,2-二置換-1,3-シクロペンタンジオンのシリルエノールエーテル化によって得られる酸素置換シクロペンタジエンを拠点として、複雑なノルボルナン誘導体を合成しています。例えば、2位側鎖の3’位にジエノフィル部位を持つ化合物AからシクロペンタジエンBを経た分子内Diels–Alder反応によって三環性化合物Cの合成に成功しています。また、側鎖2’位にピコリノイルオキシ基を持つ化合物Dから7-ノルボルナノン誘導体Eに導くことに成功しています。後者の反応は、シクロブタン環の形成によって得られる二環性化合物Fの転位反応を経由しており、非常にユニークです。現在、本知見を生かして、他の複雑なノルボルナン化合物の合成を検討しています。
ヘテロ環を持つ新規生物活性分子の創製
これまで上市されている低分子医薬品の多くには、窒素や酸素をはじめとするヘテロ原子が炭素環に組み込まれたヘテロ環を含んでいます。これは、創薬研究において標的となる生体分子との相互作用を増大させるために、ヘテロ原子をリガンド上に導入する手法が一般的に用いられるからです。そのため、ヘテロ環を持つ新規生物活性分子の創出は創薬研究においてとても重要です。
私たちはプリン骨格を持つヒポキサンチンに窒素が組み込まれた2-アザヒポキサンチン(AHX)に着目しています。AHXは静岡大学に河岸先生らがフェアリーリング惹起物質として単離した天然物でありますが、植物成長促進作用を示すことが明らかになっています。また、AHXの類縁体の中には化粧品原料として使用されているため、AHX類は創薬研究の基礎研究に打って付けの化合物です。現在、顕著な生物活性を持つAHX類縁体の創製を目指した研究を行っています。

これまでの研究
複雑な骨格と顕著な生物活性を持つ天然有機化合物の化学合成を中心に、合成プローブ分子を利用した生物活性物質の作用機作解明研究、生物活性物質の細胞内標的タンパク質を探索する技術の開発、特定のタンパク質に結合する小分子リガンドの探索方法の開発、小分子酸化酵素シトクロムP450の典型的基質の探索法の開発などを行ってきました。
特異な骨格と顕著な生物活性を持つ天然有機化合物の化学合成
生物活性を発現する有機分子の構造や、活性発現の仕組みを理解するための方法として、その構造を1から合成するアプローチ(全合成)があります。これは古典的で手間も時間もかかる方法ですが、多くの利点を持ちます。即ち、(1)提唱された構造が正しいかどうか(論文で提唱されている化合物構造には時々誤りがあります)を確認できる、(2)その物質が希少だった場合、供給する経路を確立できる、(3)関連化合物の供給が可能となり、どの部分構造が生物活性にどの位重要かの情報(構造活性相関情報)を得ることができる、などです。一方、自然が提示する天然有機化合物(天然物)の複雑な造形を、効率的に、美しく作りたい、という、純粋かつ根源的な動機もあります。
これらの動機を元に、これまでに、神経成長因子産生促進作用を持つジテルペンsabronine Gや、動物細胞に特異な液胞化を誘導するvicenistatin、抗腫瘍性マクロライドFD-891とFD-892、ある種の細胞膜脂質と特異的に相互作用する抗真菌マクロラクタムheronamide類などの合成研究を行い、化学合成を達成しました。

生物活性天然物の構造活性相関研究
全合成研究で確立した合成経路を元に、各種の誘導体を合成し、構造活性相関を明らかにしました。また、破骨細胞の前駆細胞から破骨細胞への分化を阻害する化合物methyl gerfelinの系統的な構造活性相関研究を行い、その生物活性に関わる標的タンパク質への選択性を高めた化合物の創製に成功しました。

合成プローブ分子を用いた生物活性物質の作用機作解析
生物活性を持つ有機分子が、生体内のどのような分子に作用して効果を発揮するかを知ることは、新しい薬を創製するために大変です。しかし、多くの場合、生物活性分子そのものは検出できない場合が多く、細胞のどこに局在するかや、どのような生体分子と結合するかを知るには、合成化学の力を使って、生物活性分子に細工を施し、検出できるようにする方法が取られます。これをプローブ化と言い、合成した分子をプローブ分子と言います。
これまでに、破骨細胞選択的にアポトーシスを誘導する天然物リベロマイシンAや、タンパク質脱リン酸化酵素2A(PP2A)選択的阻害剤phoslactomycin、実験動物において大腸癌の発がんを抑える化合物GO-Y030の合成プローブを創製し、用いることで、これらの化合物の生物活性発現機構の解明を行いました(理化学研究所、東北大学、秋田大学との共同研究)。

生物活性物質の細胞内標的タンパク質を探索する技術の開発
生物活性を持つ有機分子が細胞内で生物活性を発現する際、主な相手(標的)となるのがタンパク質です。これを標的タンパク質と呼びます。生物活性化合物がどのようなタンパク質を標的タンパク質とするかを探索する方法として、分子の釣り竿(アフィニティー樹脂)に、生物活性化合物を餌として固定化し、この釣り竿を用いて、多数のタンパク質の混合物(細胞抽出液)から標的タンパク質を釣る方法があります。我々は、ジアジリンと呼ばれる官能基の光照射によって発生するカルベンと呼ばれる高反応性中間体を利用して、多様な生物活性化合物を分子の釣り竿に固定化する方法(光親和型小分子固定法)を開発しました。また、このように作成した釣り竿を用いて生物活性物質の細胞内標的タンパク質を探索する方法を開発しました。また、釣り竿と、餌となる小分子とを繋ぐ分子の糸の部分に、特定の刺激によって切れる仕組みを導入した、第二世代、第三世代の釣り竿を開発しました。

特定のタンパク質に結合する小分子リガンドの探索方法の開発

上記で開発した分子の釣り竿を使えば、一種類の生物活性化合物に対する標的タンパク質を、多数のタンパク質の中から釣り上げることができます。一方、逆に、特定のタンパク質に対して強く結合する有機分子(リガンド、と呼びます)が取得できれば、それらの中には、そのタンパク質の機能を効果的に制御する化合物があるはずです。このような観点から、光親和型小分子固定法を用いて、多種類の有機小分子を微小チップに固定化した化合物のマイクロアレイを作成しました。いわば、様々な餌がつけられた、分子の延縄漁法です。この方法を用いて、様々な疾患関連タンパク質リガンドの探索が行われています。
小分子酸化酵素シトクロムP450に対する典型的基質の探索法の開発
小分子酸化酵素シトクロムP450は、生体内で、有機小分子の解毒代謝や資化(その分子を栄養源として利用すること)、有用な二次代謝産物の生合成など、様々な重要な機能を担うタンパク質群です。また、有用な有機小分子を産生するため、人工的に機能改変を行ったP450群も創製されています。しかしながら、どのようなP450タンパク質がどのような有機小分子を効率的に酸化し、どのような分子に変換するかを知る良い方法は未だにありません。
そこで我々は、自身で開発した発蛍光プローブなどを用いた4種類の基質判定法を組み合わせることで、研究対象とするP450タンパク質の典型的良基質を、化合物ライブラリーから探索する統合的基質判定法を開発しました。
本方法を用いれば、どのようなP450タンパク質が、どのような小分子を良い基質として認識して酸化するかが分かるため、このような知見を蓄積すれば、将来的には、小分子の有用酸化試薬としてP450タンパク質ライブラリ−の整備や、目的の有機小分子の望みの部分を酸化できる人工P450タンパク質のデザインが可能になると考えられます。

生物活性分子に新規機能を付与する試薬の開発
生物活性を持つ有機分子に自在に官能基を導入できれば、その分子に新しい機能を付与することができます。その結果、薬効の増強や他の分子との複合体形成が可能となります。我々は、生物活性分子や天然物に広く含まれる芳香環に、簡便かつ穏和な条件でプロパルギル基を導入できる方法や試薬を開発しました。プロパルギル基は末端アルキン(炭素―炭素三重結合)を持つため、クリック反応による他の分子との連結や、ラマンイメージングを用いた細胞内局在観察への応用が可能となります。

これまでの研究(池内)
構造多様性を持つエラジタンニンの合成研究
エラジタンニンは1,000種類以上の化合物が属するポリフェノール化合物群の総称であり、そのほとんどがD-グルコース、ガロイル基(青色)、ヘキサヒドロキシジフェノイル基(赤色)、そしてジアリールエーテル構造(緑色)を持っています。抗酸化・抗菌作用をはじめとする多種多様な生物活性を示し、ゲンノショウコのようなエラジタンニンを含む植物が漢方薬として用いられているなど、新規医薬品のシード候補といえます。しかし、類似の構造様式を持つ天然物が多数含まれること、化学合成が困難なことが創薬化学研究へ展開する上で課題となっています。私は、2015年から関西学院大学山田英俊研究室で3年間エラジタンニンの統一的合成を目指した研究に参画し、下図に示す天然物及び類縁体の合成に成功しました。また、ジアリールエーテル構造を構築する方法として、オルトキノンモノケタールを用いたフェノールのoxa-Michael付加・脱離及び還元的芳香化を経る方法論を開発しました。この方法は、立体的に非常に混み合ったオルト四置換ジアリールエーテル構造を持つ構成基も構築可能です。

有機合成に有用な保護基の開発
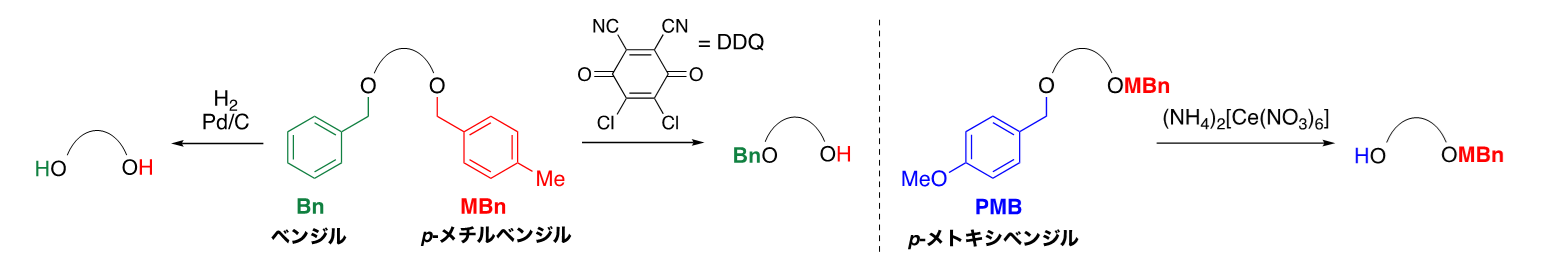
有機合成ではアルコールなど多数の官能基を保護する必要が頻出するので、これまでに多種多様な保護基が開発されています。私たちは、アルコール保護基として汎用されているベンジル(Bn)基にメチル基を導入したp-メチルベンジル(MBn)基が有機合成に有用なアルコール保護基であることを明らかにしました。
Bn基は接触水素化条件で容易に除去できますが、二重結合など接触水素化条件に持たない官能基を残しながらBn基を除去する場合は、同じ反応条件を利用できません。一方、MBn基は接触水素化条件だけでなく、2,3-ジクロロ-5,6-ジシアノ-1,4-ベンゾキノン(DDQ)を用いる酸化条件でも除去可能な保護基ですので、上記の問題はMBn基を利用することで解決できます。Bn基アナログとして汎用されているp-メトキシベンジル(PMB)基も酸化条件で除去できますが、MBn基やBn基に比べて化学的安定性は劣っています。私たちはこのPMB基の性質を逆手にとり、酸化剤にDDQより酸化力が劣る(NH4)2[Ce(NO3)6]を用いることで、MBn基共存下でPMB基のみを選択的に除去することにも成功しています。